Rayos Catódicos:Historia, Naturaleza y Caracteristicas
Rayos Catódicos:Historia, Naturaleza y Sus Caracteristicas
LOS RAYOS CATÓDICOS: Michael Faraday, después de haber entendido bien el fenómeno eléctrico, después de haber demostrado que el agua en la que se ha diluido una buena cantidad de sal es una buena conductora de la corriente eléctrica y después de haber comprendido perfectamente el fenómeno de la electrolisis, quiso saber si los gases y el vacío también eran conductores de la electricidad.
Había construido tubos con un cátodo y un ánodo, es decir, unidos ambos a los dos bornes de una pila Volta o a los de uno de esos generadores de electricidad que acababa de inventar.
Previamente había hecho el vacío en el tubo.
De hecho, era un vacío muy malo y el tubo quedaba lleno de gas diluido, pero él no llegó a darse cuenta.
Al conectar la corriente observó un resplandor macilento que se extendía desde el cátodo al ánodo (es lo que se emplea hoy en día para la iluminación mediante los tubos de neón).
Enseguida se llamó a este resplandor «rayos catódicos».
¿Cuál era la naturaleza de este resplandor?
Los sucesores de Faraday comenzaron a enfrentarse a este interrogante.
Para el inglés Crookes, que había mejorado mucho el montaje de Faraday, se trataba de partículas, de una especie de iones como los que se forman en la electrolisis, que, al encontrarse con el vacío residual, creaban el resplandor.
Para el alemán Lenard, alumno de Hertz (el «descubridor» de las ondas electromagnéticas), se trataba, por supuesto, de ondas.
Las ondas excitaban el vacío residual y creaban la luz macilenta.
Por ambas partes se intercambiaban argumentos y afirmaciones pocos amables, tanto que la disputa adquirió rápidamente aires de rivalidad nacional, una lucha germano-inglesa.
 Sin embargo, fue un joven francés, Jean Perrin, por entonces catedrático auxiliar en el laboratorio de Física de La Escuela Normal Superior (lugar destacado de la Física francesa), quien presentó en 1895 el argumento decisivo en favor de las partículas cargadas.
Sin embargo, fue un joven francés, Jean Perrin, por entonces catedrático auxiliar en el laboratorio de Física de La Escuela Normal Superior (lugar destacado de la Física francesa), quien presentó en 1895 el argumento decisivo en favor de las partículas cargadas.
Con la ayuda de un imán desvía los rayos catódicos (el resplandor macileto) y, colocando una caja de Faraday, es decir, una caja metálica donde les rayos chocan con el tubo, recupera una corriente eléctrica que procede a medir.
Por lo tanto es cierto que los rayos catódicos están formados por una corriente eléctrica, es decir, por un flujo de partículas cargadas de electricidad. Como en la electrolisis.
De buenas a primeras, J. J. Thomson se vuelca en el experimento de Perrin, pero ahora desvía los rayos catódicos no sólo mediante un campo magnético, sino también con un campo eléctrico.
Entonces se piensa que los rayos catódicos son una especie de iones.
Las descargas eléctricas en los tubo de vacío serían de este modo la manifestación de una electrolisis gaseosa.
 Entonces Thomson, mediante fórmulas matemáticas del electromagnetismo, calcula la relación entre la carga eléctrica y la masa de esas partículas, midiendo las desviaciones de los rayos en función de la intensidad de los campos magnético y eléctrico que se aplican.
Entonces Thomson, mediante fórmulas matemáticas del electromagnetismo, calcula la relación entre la carga eléctrica y la masa de esas partículas, midiendo las desviaciones de los rayos en función de la intensidad de los campos magnético y eléctrico que se aplican.
A ello añade una hipótesis de trabajo interesante: si se toma como valor de la carga eléctrica la caga elemental de electricidad determinada por Faraday en sus experimentos de electrolisis, la masa obtenida para la partícula cargada es pequeñísima 1.800 veces más pequeña que la del átomo más ligero, el del hidrógeno.
Por lo tanto, esas partículas que van del cátodo al ánodo no son ni átomos ni iones, como en la electrólisis.
¿Qué son entonces?.
Thomson no lo sabe muy bien, pero sugiere que se las llame corpúsculos, palabra que muy pronto quedará olvidada ante la de electrones (portadores de electricidad).
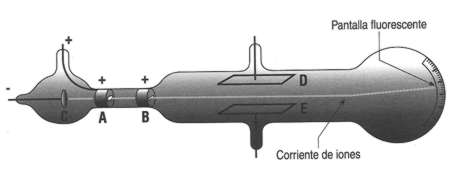
Un tubo de descarga de Thompson.
Un haz de rayos catódicos emitido por el cátodo C se focaliza en A y B y pasa entre D y E, donde hay un campo eléctrico.
Se crea un campo magnético perpendicular al campo eléctrico mediante bobinas colocadas en el exterior del tubo (según E. Segré).
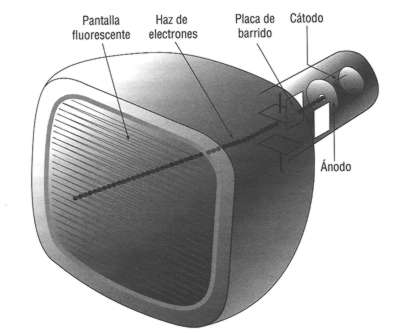
Los tubos de rayos catódicos, llamados más corrientemente tubos catódicos, se utilizan en los aparatos de televisión.
Thompson, como hemos visto, determinaba la trayectoria de dichos rayos (invisibles) a partir del punto luminoso producido por la interacción entre esos rayos y la pared del tubo de vidrio.
El punto luminoso sirve hoy en día para formar la imagen en la pantalla fluorescente de los tubos catódicos.
Un tubo de televisión es un tubo catódico dirigido hacia el telespectador.
En el tubo, los rayos quedan desviados por fuerzas eléctricas y barren la pantalla fluorescente.
Cuando ésta, recubierta de una capa especial, recibe los rayos catódicos, se forma un punto luminoso.
La señal de televisión dirige la intensidad de los rayos en cada momento, de tal forma que se hace aparecer en pantalla puntos luminosos o sombras.
La lentitud del cerebro y del ojo con relación a esas estructuras cambiantes nos permite tener una visión global de la imagen producida (según Steve Weinberg).
Pero ¿de dónde vienen esos electrones?.
No pueden provenir más que del cátodo.
Así pues, el cátodo, sólido y metálico, contiene electrones capaces de desprenderse de él.
Por lo tanto, los electrones son partículas cargadas de electricidad negativa y constitutivos esenciales de la materia sólida.
Los rayos catódicos no son ondas, sino partículas, corpúsculos de materia.
Thomson, yendo aún más lejos en este razonamiento, se pregunta: ¿no está hecha la materia más que de electrones?.
Entonces construye un modelo de átomo según el cual los electrones desempeñan un papel esencial.
Para él un átomo es un conjunto de electrones que se desplazan dentro de una esfera de diámetro limitado.
Esta esfera de paredes infinitamente delgadas llevaría una carga eléctrica positiva para garantizar la neutralidad eléctrica del conjunto, y encerraría en su interior una población de electrones.
Además de que la naturaleza de las paredes cargadas de electricidad positiva sigue siendo misteriosa, Thomson tiene que enfrentarse a un problema de masa.
¡Desde los tiempos de Avogadro se sabía calcular la masa de un solo átomo en un elemento dado al tomar la masa atómica y dividirla por 6,02 1023!.
Pero ¿cómo explicar esta masa con electrones tan livianos -¡Thompson no duda en imaginar que un solo átomo encierra millares de electrones!
Fuente Consultada: Un Poco de Ciencia Para Todo El Mundo - Wikipedia - Enciclopedia de Electrónica Tomo I.
Temas Relacionados:
Usos de los Rayos Infrarrojos
Efectos de los Rayos Ultravioleta
El Atomo Composicion Energia Nuclear Electrones y Protones
Cálculo del Radio de la Orbita en el Átomo de Hidrógeno
El Atomo Para Niños y Principiantes
Teoría de Desintegración Nuclear del Átomo Radioactividad
Leyes de la Teoría Atómica
Resumen de la Teoria Atomica
Enlace Externo:• Características de los Rayos Catódicos






